Câu hỏi:
Người ta dùng 3636 nguồn giống nhau, mỗi nguồn có suất điện động \({E_0} = 1,5V\), điện trở trong \(r = 0,9\Omega \;\)để cung cấp điện cho một bình điện phân đựng dung dịch ZnSO4với cực dương bằng kẽm, có điện trở \(R = 3,6\Omega \). Mắc hỗn hợp đối xứng bộ nguồn sao cho dòng điện qua bình điện phân là lớn nhất. Tính lượng kẽm bám vào catốt của bình điện phân trong thời gian 1 giờ 4 phút 20 giây. Biết kẽm có \(A = 65,n = 2\).
A.2,35g
B.3,25g
Đáp án chính xác
C.1,625g
D.1,2g
Trả lời:
Gọi x – là số nhánh=>Số nguồn trên một nhánh là: \(y = \frac{{36}}{x}\)Ta có:+ Suất điện động của bộ nguồn: \({E_b} = y{E_0} = \frac{{36}}{x}{E_0} = \frac{{54}}{x}\)+ Điện trở trong của bộ nguồn: \({r_b} = \frac{{yr}}{x} = \frac{{\frac{{36}}{x}.0,9}}{x} = \frac{{32,4}}{{{x^2}}}\)Cường độ dòng điện qua mạch: \(I = \frac{{{E_b}}}{{R + {r_b}}} = \frac{{\frac{{54}}{x}}}{{3,6 + \frac{{32,4}}{{{x^2}}}}} = \frac{{54}}{{3,6x + \frac{{32,4}}{x}}}\)Imaxkhi mẫu minTa có:\(3,6{\rm{x}} + \frac{{32,4}}{x} \ge 2\sqrt {3,6{\rm{x}}.\frac{{32,4}}{x}} = 21,6\)Dấu “=” xảy ra khi \(3,6{\rm{x}} = \frac{{32,4}}{x} \to x = 3\)Khi đó : Imax= 2,5AKhối lượng kẽm bám vào catốt của bình điện phân trong thời gian 1 giờ 4 phút 20 giây là:\(m = \frac{1}{F}\frac{A}{n}It = \frac{1}{{96500}}\frac{{65}}{2}.2,5.(60.60 + 4.60 + 20) = 3,25g\)Đáp án cần chọn là: B
====== **** mời các bạn xem câu tiếp bên dưới **** =====
- Cho mạch điện như hình vẽ: Nguồn điện có suất điện động \(E = 12V\), điện trở trong \(r{\rm{ }} = \;1\Omega ,\;{R_2} = 12\Omega \;\)và là bình điện phân đựng dung dịch \(AgN{O_3}\)với điện cực anôt bằng bạc, \({R_1} = 3\Omega ,\;{R_3} = 6\Omega \). Cho biết bạc (Ag) có khối lượng mol là 108g/mol, hóa trị 1, hằng số Faraday F = 96500C/mol. Khối lượng bạc bám vào catot sau thời gian 16 phút 5 giây là – ĐGNL-HN
Câu hỏi:
Cho mạch điện như hình vẽ: Nguồn điện có suất điện động \(E = 12V\), điện trở trong \(r{\rm{ }} = \;1\Omega ,\;{R_2} = 12\Omega \;\)và là bình điện phân đựng dung dịch \(AgN{O_3}\)với điện cực anôt bằng bạc, \({R_1} = 3\Omega ,\;{R_3} = 6\Omega \). Cho biết bạc (Ag) có khối lượng mol là 108g/mol, hóa trị 1, hằng số Faraday F = 96500C/mol. Khối lượng bạc bám vào catot sau thời gian 16 phút 5 giây là

A.0,54g.
Đáp án chính xác
B.0,72g.
C.0,81g.
D.0,27g.
Trả lời:
Cấu tạo mạch: \(\left( {{R_2}//{R_3}} \right)nt{R_1}\)Ta có: \({R_{23}} = \frac{{{R_2}{R_3}}}{{{R_2} + {R_3}}} = \frac{{12.6}}{{12 + 6}} = 4\,\,\left( {\rm{\Omega }} \right)\)\( \Rightarrow {R_N} = {R_1} + {R_{23}} = 3 + 4 = 7\,\,\left( {\rm{\Omega }} \right)\)Áp dụng định luật Ôm cho toàn mạch, ta có:\(I = \frac{E}{{{R_N} + r}} = \frac{{12}}{{7 + 1}} = 1,5\,\,\left( A \right) = {I_1} = {I_{23}}\)Ta có: \({U_{23}} = {I_{23}}.{R_{23}} = 1,5.4 = 6\,\,\left( V \right) = {U_2} = {U_3}\)\( \Rightarrow {I_2} = \frac{{{U_2}}}{{{R_2}}} = \frac{6}{{12}} = 0,5\,\,\left( A \right)\)Khối lượng bạc bám vào catot là:\({m_{Ag}} = \frac{1}{F}.\frac{A}{n}.{I_2}t = \frac{1}{{96500}}.\frac{{108}}{1}.0,5.\left( {16.60 + 5} \right) = 0,54\,\,\left( g \right)\)Đáp án cần chọn là: A
====== **** mời các bạn xem câu tiếp bên dưới **** =====
- Cho mạch điện như hình vẽ:\(E = 9V;r = 0,5\Omega \). Bình điện phân chứa dung dịch đồng sunfat với hai cực bằng đồng. Đèn ghi 6V − 9W. Rxlà một biến trở. Điều chỉnh \({R_x} = 12\Omega \;\)thì đèn sáng bình thường. Điện trở của bình điện phân là: – ĐGNL-HN
Câu hỏi:
Cho mạch điện như hình vẽ:
 \(E = 9V;r = 0,5\Omega \). Bình điện phân chứa dung dịch đồng sunfat với hai cực bằng đồng. Đèn ghi 6V − 9W. Rxlà một biến trở. Điều chỉnh \({R_x} = 12\Omega \;\)thì đèn sáng bình thường. Điện trở của bình điện phân là:
\(E = 9V;r = 0,5\Omega \). Bình điện phân chứa dung dịch đồng sunfat với hai cực bằng đồng. Đèn ghi 6V − 9W. Rxlà một biến trở. Điều chỉnh \({R_x} = 12\Omega \;\)thì đèn sáng bình thường. Điện trở của bình điện phân là:A.\(2,5\;\Omega \;\)
B.\(4\;\Omega \;\)
C.\(3\;\Omega \;\)
D.\(1\;\Omega \;\)
Đáp án chính xác
Trả lời:
Ta có:+ Điện trở của đèn: \({R_d} = \frac{{{U^2}}}{P} = \frac{{{6^2}}}{9} = 4{\rm{\Omega }}\)+ Cường độ dòng điện qua đèn: \({I_d} = \frac{P}{U} = \frac{9}{6} = 1,5A\)+ Ud= URx= 6V=>Cường độ dòng điện qua Rx:\({I_x} = \frac{{{U_{{R_x}}}}}{{{R_x}}} = \frac{6}{{12}} = 0,5A\)Cường độ dòng điện chính trong mạch: I = Id+ Ix= 1,5 + 0,5 = 2AMặt khác: \(I = \frac{E}{{{R_N} + r}} \to {R_N} = \frac{E}{I} – r = \frac{9}{2} – 0,5 = 4{\rm{\Omega }}\)Mạch ngoài gồm: Rb( điện trở bình điện phân) nt (Rd// Rx)\({R_{dx}} = \frac{{{R_d}{R_x}}}{{{R_d} + {R_x}}} = \frac{{4.12}}{{4 + 12}} = 3{\rm{\Omega }}\)\({R_N} = {R_b} + {R_{dx}} \to {R_b} = 4 – 3 = 1{\rm{\Omega }}\)Đáp án cần chọn là: D
====== **** mời các bạn xem câu tiếp bên dưới **** =====
- Đồ thị biểu diễn sự phụ thuộc giữa khối lượng chất giải phóng ra ở điện cực của bình điện phân và điện lượng tải qua bìnhĐương lượng điện hóa của chất điện phân trong bình này là: – ĐGNL-HN
Câu hỏi:
Đồ thị biểu diễn sự phụ thuộc giữa khối lượng chất giải phóng ra ở điện cực của bình điện phân và điện lượng tải qua bình
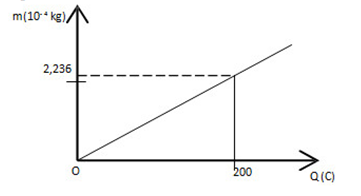 Đương lượng điện hóa của chất điện phân trong bình này là:
Đương lượng điện hóa của chất điện phân trong bình này là:A.1,18.10-6kg/C
B.1,118.10-6kg/C
Đáp án chính xác
C.2,36.10-7kg/C
D.3,262.10-6kg/C
Trả lời:
Theo định luật I – Faraday, ta có: m = kq\( \to k = \frac{m}{q} = \frac{{{{2,236.10}^{ – 4}}}}{{200}} = {1,118.10^{ – 6}}kg/C\)Đáp án cần chọn là: B
====== **** mời các bạn xem câu tiếp bên dưới **** =====
- Bình điện phân có anốt làm bằng kim loại của chất điện phân có hóa trị 2. Cho dòng điện 0,2A chạy qua bình trong 16 phút 5 giây thì có 0,064g chất thoát ra ở điện cực. Kim loại dùng làm anốt của bình điện phân là: – ĐGNL-HN
Câu hỏi:
Bình điện phân có anốt làm bằng kim loại của chất điện phân có hóa trị 2. Cho dòng điện 0,2A chạy qua bình trong 16 phút 5 giây thì có 0,064g chất thoát ra ở điện cực. Kim loại dùng làm anốt của bình điện phân là:
A.sắt
B.bạc
C.đồng
Đáp án chính xác
D.kẽm
Trả lời:
Ta có:Khối lượng chất thoát ra ở điện cực:\(m = \frac{1}{F}\frac{A}{n}It \leftrightarrow 0,064 = \frac{1}{{96500}}\frac{A}{2}.0,2.(16.60 + 5) \to A = 64\)=>Kim loại dùng làm anot của bình điện phân là đồng có số khối A = 64Đáp án cần chọn là: C
====== **** mời các bạn xem câu tiếp bên dưới **** =====
- Một bình điện phân dung dịch CuSO4có anốt làm bằng đồng, điện trở của bình điện phân \(R{\rm{ }} = {\rm{ }}8\left( \Omega \right),\)được mắc vào hai cực của bộ nguồn E = 9(V), điện trở trong\(r{\rm{ }} = {\rm{ }}1\left( \Omega \right)\). Cho ACu= 64(đvc), nCu = 2. Khối lượng Cu bám vào ca tốt trong thời gian 5h có giá trị là: – ĐGNL-HN
Câu hỏi:
Một bình điện phân dung dịch CuSO4có anốt làm bằng đồng, điện trở của bình điện phân \(R{\rm{ }} = {\rm{ }}8\left( \Omega \right),\)được mắc vào hai cực của bộ nguồn E = 9(V), điện trở trong\(r{\rm{ }} = {\rm{ }}1\left( \Omega \right)\). Cho ACu= 64(đvc), nCu = 2. Khối lượng Cu bám vào ca tốt trong thời gian 5h có giá trị là:
A.5,97 g.
Đáp án chính xác
B. 5 g.
C.11,94 g.
D.10,5 g.
Trả lời:
Cường độ dòng điện chạy qua bình điện phân là \(I = \frac{E}{{R + r}} = \frac{9}{{8 + 1}} = 1\left( A \right)\)Khối lượng Cu bám vào ca tốt trong thời gian 5h là\(m = \frac{1}{F}\frac{A}{n}It = \frac{1}{{96500}}.\frac{{64}}{2}.1.5.3600 = 5,97g\)Đáp án cần chọn là: A
====== **** mời các bạn xem câu tiếp bên dưới **** =====

Trả lời