Giải bài tập Chuyên đề Hóa học 10 Bài 3: Năng lượng hoạt hóa của phản ứng hóa học
Giải Chuyên đề Hóa học 10 trang 19
A/ Câu hỏi đầu bài
Câu hỏi mở đầu trang 19 Chuyên đề Hóa 10: Hydrogen và oxygen không phản ứng với nhau ở nhiệt độ thường, nhưng khi đưa một ít bột platinium (Pt) vào hỗn hợp hai khí đó, phản ứng xảy ra ngay tức khắc, tạo thành nước. Yếu tố nào quyết định sự thay đổi đó?
Lời giải:
Yếu tố quyết định sự thay đổi trên là chất xúc tác. Chất xúc tác có tác dụng làm tăng tốc độ phản ứng nhưng không bị biến đổi về chất và lượng sau phản ứng.
Giải Chuyên đề Hóa học 10 trang 20
B/ Câu hỏi giữa bài
I. Năng lượng hoạt hóa
Câu hỏi 1 trang 20 Chuyên đề Hóa 10: Cho phản ứng:
2NOCl(g) ⟶ 2NO(g) + Cl2(g), năng lượng hoạt hóa của phản ứng là 100kJ/mol. Ở 350K, hằng số tốc độ của phản ứng là 8.10-6 L/(mol.s). Tính hằng số tốc độ ở phản ứng ở 400 K.
Lời giải:
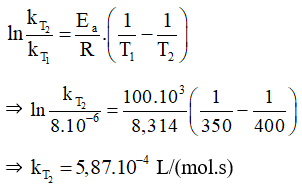
Câu hỏi 2 trang 20 Chuyên đề Hóa 10: Tính năng lượng hoạt hóa của một số phản ứng biết rằng khi nhiệt độ tăng từ 300 K lên 310 K thì tốc độ phản ứng tăng 3 lần.
Lời giải:
Khi nhiệt độ tăng từ 300 K lên 310 K thì tốc độ phản ứng tăng 3 lần.
⇒
Mà
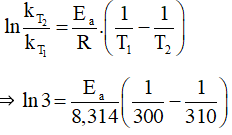
⇒ Ea = 84 944,92 J/mol ≈ 85 kJ/mol
Câu hỏi 3 trang 20 Chuyên đề Hóa 10: Thực nghiệm cho biết phản ứng: 2N2O5(g) ⟶ 4NO2(g) + O2(g) ở 45oC có hằng số tốc độ phản ứng là 8,17.10-3 s-1; Ea = 103,5kJ/mol. Tính hằng số tốc độ phản ứng tại 65oC.
Lời giải:
Ta có:
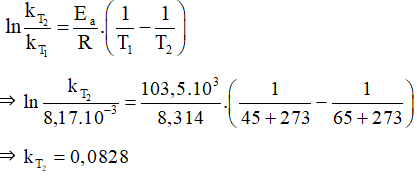
Giải Chuyên đề Hóa học 10 trang 22
II. Chất xúc tác
Câu hỏi 4 trang 22 Chuyên đề Hóa 10: Sự suy giảm tầng ozone và lỗ thủng tầng ozone (O3) đã gây ra mối lo ngại về việc gia tăng nguy cơ ung thư da, cháy nắng, mù mắt và đục thuỷ tinh thể…. Tầng ozone hấp thụ hầu hết các tia cực tím (UV) có hại cho sự sống trên Trái Đất. Các phân tử ozone có thể bị phá huỷ theo hai giai đoạn:
Cl + O3 ⟶ ClO + O2
Và ClO + O3 ⟶ Cl + 2O2
Chất xúc tác trong các quá trình này là chất nào?
Lời giải:
Chất xúc tác là Cl vì sau toàn bộ quá trình thì Cl vẫn còn nguyên, không bị biến đổi cả về chất và về lượng.
Câu hỏi 5 trang 22 Chuyên đề Hóa 10: Một phản ứng xảy ra ở 500°C, năng lượng hoạt hóa của phản ứng khi không có xúc tác và khi có xúc tác lần lượt là 55,4 kJ/mol và 13,5 kJ/mol. Chứng minh rằng chất xúc tác có ảnh hưởng đến tốc độ phản ứng.
Lời giải:
Năng lượng hoạt hóa của phản ứng khi không có xúc tác là 55,4 kJ/mol lớn hơn rất nhiều so với năng lượng hoạt hóa của phản ứng khi có xúc tác là 13,5 kJ/mol.
⇒ Chất xúc tác làm giảm năng lượng hoạt hóa, làm tăng tốc độ phản ứng.
Giải Chuyên đề Hóa học 10 trang 23
Em có thể trang 23 Chuyên đề Hóa 10: Vận dụng khái niệm năng lượng hoạt hoá để giải thích vai trò của xúc tác trong một số quá trình tự nhiên như: tiêu hoá thức ăn trong cơ thể người, động vật, … và một số quá trình sản xuất: sulfuric acid, acetic acid, rượu, bia, …
Lời giải:
– Xúc tác trong một số quá trình tự nhiên:
+ Amylase phân hủy tinh bột và carbohydrate thành đường.
+ Protease phân hủy protein thành các axit amin.
+ Lipase phân hủy lipid, là chất béo và dầu, thành glycerol và axit béo.
– Xúc tác trong một số quá trình sản xuất:
+ Hỗn hợp bột aluminium và iodine ở nhiệt độ thường không có phản ứng xảy ra, nhưng khi cho thêm một ít nước làm xúc tác, phản ứng xảy ra mãnh liệt, tạo hợp chất aluminium iodine.
2Al + 3I2 2AlI3
+ Trong các nhà máy sản xuất phân đạm người ta thường dùng sắt làm chất xúc tác để tăng tốc độ phản ứng giữa nitrogen (N2) và hydrogen (H2)
N2 + 3H2 2NH3
+ Sử dụng chất xúc tác platinium (Pt), vanadium pentoxide (V2O5) trong quá trình oxi hóa SO2 thành SO3 để sản xuất sulfuric acid (H2SO4)
2SO2 + O2 2SO3