Lý thuyết Hóa học 12 Bài 9: Amino acid và peptide
A. Lý thuyết Amino acid và peptide
I. Amino acid
1. Khái niệm và danh pháp
a) Khái niệm
– Amino acid là hợp chất hữu cơ tạp chức, trong phân tử chứa đồng thời nhóm amino ( – NH2 ) và nhóm carboxyl (-COOH)
– Các amino acid thiên nhiên hầu hết là -amino acid.
b) Danh pháp
– Tên gọi amino acid xuất phát từ tên carboxylic acid tương ứng
– Tên thay thế: chọn mạch chính chứa nhóm carboxyl, nhóm amino là nhóm thế trên mạch chính này.
– Tên bán hệ thống: vị trí của nhóm amino được kí hiệu bằng chữ cái Hy lạp (,…) và tên gọi acid được gọi theo tên thông thường.
– Ngoài ra, một số amino acid trong thiên nhiên là:
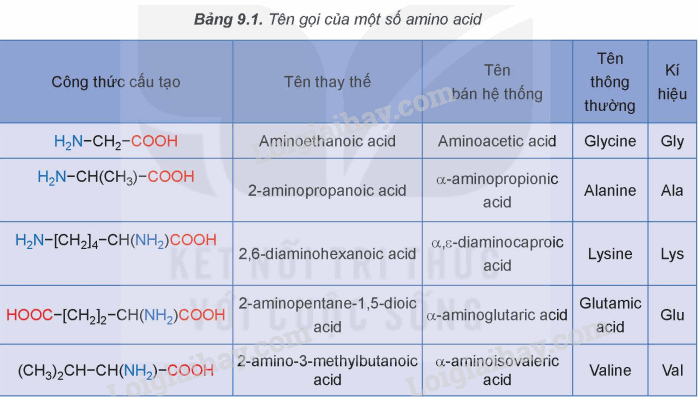
2. Đặc điểm cấu tạo
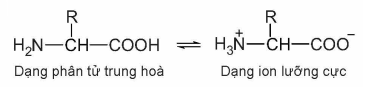
– Các amino acid tồn tại chủ yếu ở dạng ion lưỡng cực do tương tác giữa nhóm – COOH và nhóm – NH2
3. Tính chất vật lí
– Ở điều kiện thường, các amino acid là chất rắn, khi ở dạng tinh thể chúng không có màu, có nhiệt độ nóng chảy cao và thường tan tốt trong nước vì chúng tồn tại ở dạng ion lưỡng cực.
4. Tính chất hóa học
a) Phản ứng ester hóa
– Tương tự carboxylic acid, amino acid phản ứng được với alcohol tạo ester.
![]()
b) Tính chất lưỡng tính
– Nhóm amino có tính base và nhóm carboxyl có tính acid nên các amino acid có tính lưỡng tính, có thể tác dụng với acid mạnh như base mạnh.

c) Tính chất điện li
– Các amino acid có khả năng di chuyển khác nhau trong điện trường tùy thuộc vào PH của môi trường (tính chất điện li)
d) Phản ứng trùng ngưng
– Khi đun nóng, các – amino acid hoặc – amino acid có thể phản ứng với nhau để tạo thành polymer, đồng thời tách ra các phân tử nước (phản ứng trùng ngưng).
Ví dụ: Phản ứng trùng ngưng tổng hợp polycaproamide (capron) từ 6 – aminohexanoic acid.
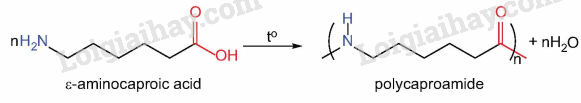
II. Peptide
1. Khái niệm
– Peptide là những hợp chất hữu cơ được cấu tạo từ các đơn vị -amino acid liên kết với nhau qua liên kết peptide ( – CO – NH – )
– Các peptide chứa từ 2, 3, 4,… đơn vị -amino acid lần lượt được gọi là dipeptide, tripeptide, tetrapeptide,…; peptide chứa nhiều đơn vị -amino acid được gọi là polypeptide
2. Cấu tạo
– Cấu tạo của một peptide được xác định bằng thứ tự liên kết của các -amino acid trong phân tử. Mỗi peptide mạch hở bắt đầu bằng amino acid đầu N và kết thúc bằng amino acid đầu C
– Tên viết tắt của peptide gồm tên viết tắt của các amino acid theo thứ tự từ amino acid đầu N đến amino acid đầu C
3. Tính chất hóa học
a) Phản ứng thủy phân
– Peptide bị thủy phân bởi acid, base hoặc enzyme. Qúa trình thủy phân không hoàn toàn có thể tạo thành các peptide nhỏ hơn
Ví dụ: Tetrapeptide Gly – Tyr – Val – Ala khi bị thủy phân không hoàn toàn có thể tạo thành các tripeptide Gly – Tyr – Val, Tyr – Val – Ala và các dipeptide là Gly – Tyr, Tyr – Val, Val – Ala.
– Trong môi trường acid hoặc môi trường base, các amino acid sẽ tác dụng với acid hoặc base để tạo thành muối tương ứng.

b) Phản ứng màu biuret
Các peptide có từ hai liên kết peptide trở lên phản ứng với thuốc thử biuret (Cu(OH)2 trong môi trường kiềm), tạo thành dung dịch có màu tím đặc trưng. Phản ứng àny được sử dụng để nhận biết các peptide (Trừ dipeptide).
Sơ đồ tư duy Amino acid và peptide
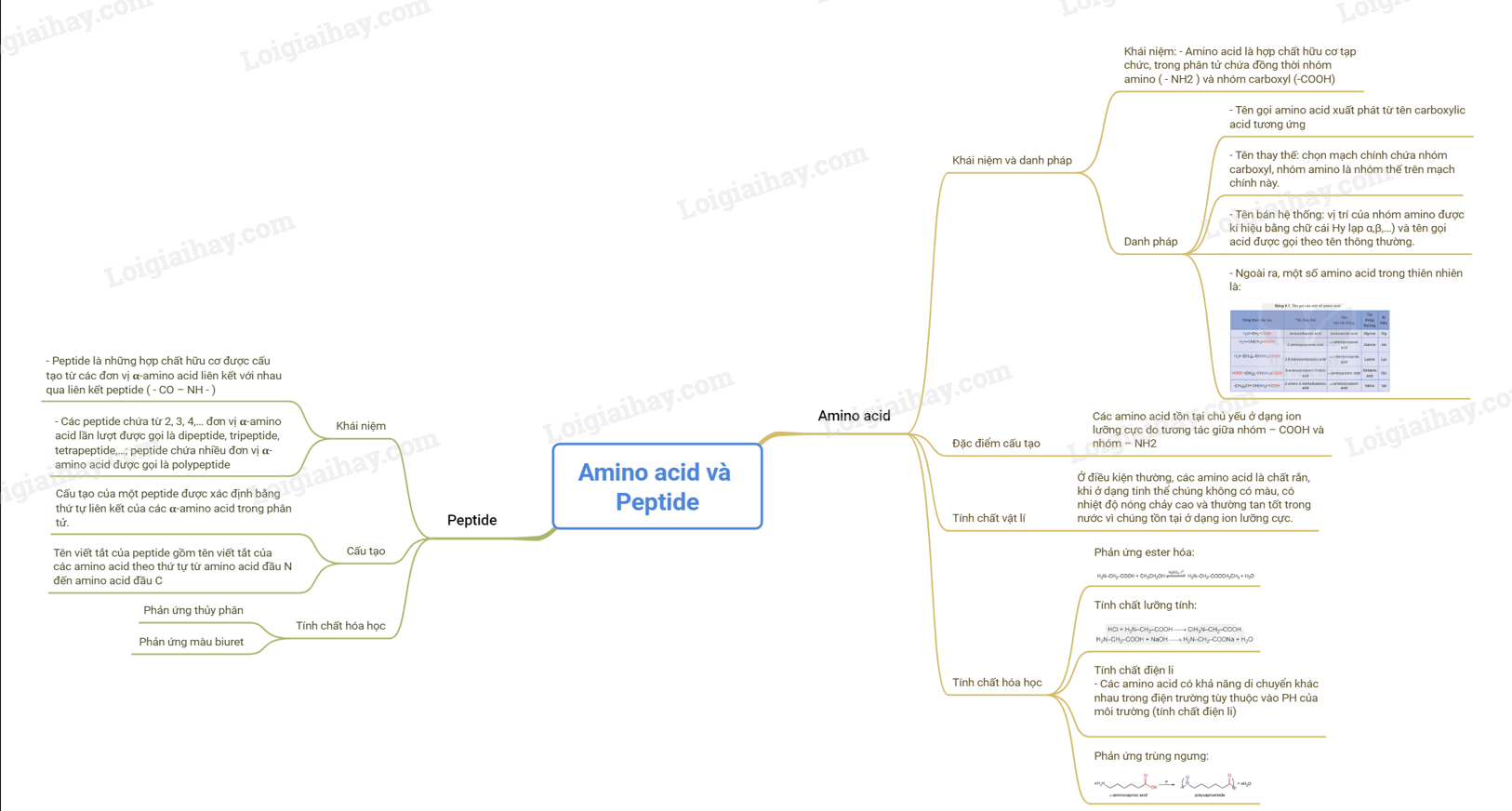
B. Trắc nghiệm Amino acid và peptide
Câu 1. Cho hai hợp chất hữu cơ X, Y có cùng công thức phân tử là C3H7NO2. Khi phản ứng với dung dịch NaOH, X tạo ra H2NCH2COONa và chất hữu cơ Z; còn Y tạo ra CH2=CHCOONa và khí T. Các chất Z và T lần lượt là
A. CH3OH và NH3.
B. CH3OH và CH3NH2.
C. CH3NH2 và NH3.
D. C2H5OH và N2.
Hướng dẫn giải
Đáp án đúng là: A
X: H2NCH2COOCH3 + NaOH → H2NCH2COONa + CH3OH (Z).
Y: CH2=CHCOONH4 + NaOH → CH2=CHCOONa + NH3 (T) + H2O.
Câu 2. Amino acid X chứa một nhóm −NH2 và một nhóm −COOH trong phân tử. Y là ester của X với alcohol đơn chức, MY = 89. Công thức của X, Y lần lượt là
A. H2N−CH2−COOH, H2N−CH2−COOCH3.
B. H2N−[CH2]2−COOH, H2N−[CH2]2−COOC2H5.
C. H2N−[CH2]2−COOH, H2N−[CH2]2−COOCH3.
D. H2N−CH2−COOH, H2N−CH2−COOC2H5.
Hướng dẫn giải
Đáp án đúng là: A
MY = 89 ⇒ Y: C3H7O2N, Y là ester của amino acid ⇒ Y: H2N−CH2−COOCH3
⇒ X: H2N−CH2−COOH.
Câu 3. Số nhóm amino và số nhóm carboxyl có trong một phân tử glutamic acid tương ứng là
A. 1 và 2.
B. 1 và 1.
C. 2 và 1.
D. 2 và 2.
Hướng dẫn giải
Đáp án đúng là: A
Glutamic acid có công thức là: HOOC(CH2)2CH(NH2)COOH ⟹ có 1 nhóm amino (NH2) và 2 nhóm carboxyl (COOH).
Câu 4. Cho các phản ứng:
H2N–CH2–COOH + HCl → Cl–H3N+–CH2–COOH
H2N–CH2–COOH + NaOH → H2N–CH2–COONa + H2O.
Hai phản ứng trên chứng tỏ aminoacetic acid
A. chỉ có tính base.
B. chỉ có tính acid.
C. có tính oxi hoá và tính khử.
D. có tính chất lưỡng tính.
Hướng dẫn giải
Đáp án đúng là: D
Hai phản ứng trên đã cho aminoacetic acid tác dụng với acid và base, điều này chứng tỏ aminoacetic acid có tính lưỡng tính.
Câu 5. Amino acid X có phân tử khối bằng 75. Tên của X là
A. alanine.
B. glycine.
C. valine.
D. lysine.
Hướng dẫn giải
Đáp án đúng là: B
X là glycine: H2NCH2COOH, có phân tử khối bằng 75.
Câu 6. Hợp chất H2NCH2COOH có tên gọi là
A. valine.
B. lysine.
C. alanine.
D. glycine.
Hướng dẫn giải
Đáp án đúng là: D
Hợp chất H2NCH2COOH có tên gọi là glycine.
Câu 7. Số liên kết peptide có trong một phân tử Ala-Gly-Val-Gly-Ala là
A. 4.
B. 5.
C. 3.
D. 2.
Hướng dẫn giải
Đáp án đúng là: A
Ala-Gly-Val-Gly-Ala là pentapeptide, có 4 liên kết peptide trong phân tử.
Câu 8. Chất nào sau đây là tripeptide?
A. Val-Gly.
B. Ala-Val.
C. Gly-Ala-Val.
D. Gly-Ala.
Hướng dẫn giải
Đáp án đúng là: C
Gly-Ala-Val là tripeptide, chứa 3 đơn vị α-amino acid.
Câu 9. Thủy phân không hoàn toàn tetrapeptide X mạch hở, thu được hỗn hợp sản phẩm có Gly-Ala, Phe-Val và Ala-Phe. Cấu tạo của X là
A. Gly-Ala-Val-Phe.
B. Ala-Val-Phe-Gly.
C. Val-Phe-Gly-Ala.
D. Gly-Ala-Phe-Val.
Hướng dẫn giải
Đáp án đúng là: D
X là tetrapeptide nên gồm 4 gốc ⟹ Phe và Ala phải trùng nhau trong các dipeptide tạo thành ⟹ X: Gly-Ala-Phe-Val.
Câu 10. Thủy phân hoàn toàn 1 mol pentapeptide X, thu được 2 mol glycine (Gly), 1 mol alanine (Ala), 1 mol valine (Val) và 1 mol phenylalanine (Phe). Thủy phân không hoàn toàn X thu được dipeptide Val-Phe và tripeptide Gly-Ala-Val nhưng không thu được dipeptide Gly-Gly. Chất X có công thức là
A. Gly-Phe-Gly-Ala-Val.
B. Gly-Ala-Val-Val-Phe.
C. Gly-Ala-Val-Phe-Gly.
D. Val-Phe-Gly-Ala-Gly.
Hướng dẫn giải
Đáp án đúng là: C
Vì X chỉ chứa 1Val nên Val trong các peptide tạo thành phải trùng nhau ⟹ X chứa : Gly-Ala-Val-Phe.
X không chứa Gly-Gly nên X là Gly-Ala-Val-Phe-Gly.
Câu 11. Xét phân tử valine.
a. Công thức cấu tạo thu gọn của valine là (CH3)2CH–CH(NH2)COOH.
b. Ở điều kiện thường, valine tồn tại chủ yếu ở dạng ion lưỡng cực.
c. Ở điều kiện thường, valine là chất rắn, khi ở dạng kết tinh thì có màu trắng.
d. Valine có tính lưỡng tính.
Hướng dẫn giải
a. Đúng.
b. Đúng.
c. Sai vì ở dạng kết tinh thì valine không màu.
d. Đúng.
Câu 12. Thí nghiệm về phản ứng màu biuret của peptide.
– Bước 1: Cho khoảng 1 mL dung dịch NaOH 30
– Bước 2: Cho khoảng 4 mL dung dịch lòng trắng trứng (polypeptide) vào ống nghiệm, lắc đều.
a. Sau bước 1 thu được dung dịch xanh lam.
b. Sau bước 2 thu được dung dịch màu tím.
c. Nếu thay lòng trắng trứng (polypeptide) bằng các dipeptide khác thì hiện tượng sau bước 2 không đổi.
d. Phản ứng này có thể dùng để phân biệt lòng trắng trứng với các dipeptide.
Hướng dẫn giải
a. Sai vì sau bước 1 thu được kết tủa xanh lam.
b. Đúng vì xảy ra phản ứng màu biuret tạo dung dịch màu tím.
c. Sai vì dipeptide không có phản ứng này nên ở bước 2 không thu được hiện tượng như thí nghiệm trên.
d. Đúng vì lòng trắng trứng có phản ứng trên còn dipeptide thì không.
Câu 13. Hợp chất hữu cơ X (C5H11NO2) tác dụng với dung dịch NaOH dư, đun nóng, thu được muối sodium của α-amino acid và alcohol. X có bao nhiêu công thức cấu tạo thỏa mãn?
Hướng dẫn giải
Đáp số 5.
Các công thức cấu tạo thỏa mãn là:
H2N–CH2–COOCH2CH2CH3; H2N–CH2–COOCH(CH3)2; CH3–CH(NH2)–COOC2H5; CH3–CH2–CH(NH2)–COOCH3; (CH3)2–C(NH2)–COOCH3.
Câu 14. Cho X là Ala-Gly-Ala-Val-Gly-Val và Y là Gly-Ala-Gly-Glu. Thủy phân hoàn toàn m gam hỗn hợp gồm X và Y thu được 4 amino acid, trong đó có 30 gam glycine và 28,48 gam alanine. Giá trị của m là
Hướng dẫn giải
Đáp số: 83,2.
Câu 15. Cho 15 gam H2N–CH2–COOH tác dụng vừa đủ với dung dịch HCl thu được m gam muối. Giá trị của m là bao nhiêu?
Hướng dẫn giải
Đáp số 22,3.
PTHH: H2N – CH2 – COOH + HCl ⟶ ClH3N – CH2 – COOH
0,2 0,2 (mol).
mmuối = 0,2 × (35,5 + 3 + 14 + 12 + 2 + 12 + 32 + 1) = 22,3 gam.
Xem thêm các bài tóm tắt lý thuyết Hóa học lớp 12 Kết nối tri thức hay, chi tiết khác:
Lý thuyết Bài 8: Amine
Lý thuyết Bài 9: Amino acid và peptide
Lý thuyết Bài 10: Protein và enzyme
Lý thuyết Bài 12: Đại cương về polymer
Lý thuyết Bài 13: Vật liệu polymer
Lý thuyết Bài 15: Thế điện cực và nguồn điện hoá học