Giải bài tập KHTN lớp 8 Bài 10: Oxide
Giải KHTN 8 trang 44
Mở đầu trang 44 Bài 10 KHTN 8: Tại sao vôi sống (CaO) lại được sử dụng để khử chua đất trồng trọt?
Trả lời:
Khi bón vôi sống (CaO) lên ruộng, vôi sống tác dụng với nước tạo thành Ca(OH)2:
CaO + H2O → Ca(OH)2.
Ca(OH)2 tác dụng với acid có trong đất, khử chua cho đất.
I. Khái niệm
Hoạt động trang 44 KHTN 8: Tìm hiểu về khái niệm oxide
Bảng 10.1. Tên, công thức hoá học của một số oxide
|
Tên oxide (1) |
Công thức hoá học (2) QUẢNG CÁO |
Tên oxide (3) |
Công thức hoá học (4) |
|
Barium oxide |
BaO |
Carbon dioxide |
CO2 |
|
Zinc oxide |
ZnO |
Sulfur trioxide |
SO3 |
|
Aluminium oxide |
Al2O3 |
Diphosphorus pentoxide |
P2O5 |
Nhận xét thành phần nguyên tố trong công thức phân tử của các oxide ở cột (2), (4) và thực hiện các yêu cầu:
1. Đề xuất khái niệm về oxide.
2. Phân loại oxide.
Trả lời:
Nhận xét: Công thức phân tử của các oxide ở cột (2), (4) đều có chứa 2 nguyên tố, trong đó có 1 nguyên tố là oxygen (O).
1. Khái niệm oxide: Oxide là hợp chất của hai nguyên tố trong đó có một nguyên tố là oxygen.
2. Phân loại oxide:
– Dựa vào thành phần nguyên tố, oxide có thể phân thành hai loại: oxide kim loại và oxide phi kim.
– Dựa vào tính chất hoá học, oxide có thể phân thành 4 loại: oxide acid; oxide base; oxide lưỡng tính và oxide trung tính.
Giải KHTN 8 trang 45
Câu hỏi trang 45 KHTN 8: Cho các sơ đồ phản ứng sau:
(1) .. ? .. + O2 Al2O3
(2) P + .. ? .. P2O5
(3) S + .. ? .. SO2
(4) Mg + O2 .. ? ..
Hoàn thành các phương trình hoá học và đọc tên các sản phẩm tạo thành.
Trả lời:
(1) 4Al + 3O2 → 2Al2O3 (aluminium oxide)
(2) 4P + 5O2 → 2P2O5 (diphosphorus pentoxide)
(3) S + O2 → SO2 (sulfur dioxide)
(4) 2Mg + O2 → 2MgO (magnesium oxide)
Hoạt động trang 45 KHTN 8: Tìm hiểu tính chất hoá học của oxide acid
Chuẩn bị: dung dịch hydrochloric acid HCl 0,1 M, thìa lấy hoá chất, ống thuỷ tinh hình chữ L, nút cao su, ống nghiệm (1) đựng khoảng 1 gam đá vôi (CaCO3) đã đập nhỏ, ống nghiệm (2) đựng nước vôi trong (Ca(OH)2).
Tiến hành:
Cho vào ống nghiệm (1) khoảng 3 ml dung dịch hydrochloric acid 0,1 M để điều chế khí carbon dioxide, đậy ống nghiệm bằng nút cao su có ống thuỷ tinh hình chữ L xuyên qua. Dẫn khí carbon dioxide vào ống nghiệm (2). Quan sát.
Thực hiện các yêu cầu:
Nêu hiện tượng xảy ra khi mới dẫn khí carbon dioxide vào nước vôi trong và khi dẫn khí carbon dioxide vào nước vôi trong một khoảng thời gian.
Trả lời:
Dẫn từ từ khí carbon dioxide vào nước vôi trong, ban đầu dung dịch vẩn đục; Tiếp tục dẫn khí carbon dioxide vào sau một khoảng thời gian vẩn đục lại tan dần.
Giải KHTN 8 trang 46
Câu hỏi trang 46 KHTN 8: Viết phương trình hoá học của phản ứng giữa SO2 và dung dịch NaOH minh hoạ cho tính chất hoá học của sulfur dioxide.
Trả lời:
Phương trình hoá học:
SO2 + 2NaOH (dư) → Na2SO3 + H2O
SO2 (dư) + NaOH → NaHSO3.
Hoạt động trang 46 KHTN 8: Tìm hiểu tính chất hoá học của oxide base
Chuẩn bị: CuO (bột); dung dịch H2SO4 loãng; thìa lấy hoá chất, ống nghiệm.
Tiến hành:
Cho vào ống nghiệm 1 thìa nhỏ bột CuO, thêm vào khoảng 3 mL dung dịch H2SO4, lắc đều ống nghiệm và quan sát.
Thực hiện yêu cầu:
Nêu hiện tượng của thí nghiệm trên và giải thích.
Trả lời:
Hiện tượng: Bột CuO tan dần, sau phản ứng dung dịch thu được có màu xanh.
Giải thích: CuO là oxide base, tác dụng với acid tạo thành muối và nước:
CuO + H2SO4 → CuSO4 + H2O.
Giải KHTN 8 trang 47
Câu hỏi 1 trang 47 KHTN 8: Viết phương trình hoá học minh hoạ cho tính chất hoá học của oxide base và oxide acid. Lấy magnesium oxide và sulfur dioxide làm ví dụ.
Trả lời:
– Tính chất hoá học của oxide base: Tác dụng với dung dịch acid tạo thành muối và nước. Ví dụ:
MgO + 2HCl → MgCl2 + H2O
MgO + H2SO4 → MgSO4 + H2O.
– Tính chất hoá học của oxide acid: Tác dụng với dung dịch base tạo thành muối và nước. Ví dụ:
SO2 + 2KOH → K2SO3 + H2O
SO2 + Ca(OH)2 → CaSO3 + H2O.
Câu hỏi 2 trang 47 KHTN 8: Cho các oxide sau: CaO, Fe2O3, SO3, CO2, CO. Oxide nào có thể tác dụng với:
a) Dung dịch HCl;
b) Dung dịch NaOH.
Viết các phương trình hoá học. Hãy cho biết các oxide trên thuộc loại oxide nào?
Trả lời:
a) Oxide tác dụng với HCl là: CaO; Fe2O3 (các oxide base).
CaO + 2HCl → CaCl2 + H2O
Fe2O3 + 6HCl → 2FeCl3 + 3H2O.
b) Oxide tác dụng với NaOH là: SO3; CO2 (các oxide acid).
SO3 + 2NaOH → Na2SO4 + H2O
CO2 + 2NaOH → Na2CO3 + H2O
Còn lại CO là oxide trung tính, không tác dụng với NaOH và HCl.
Lý thuyết KHTN 8 Bài 10: Oxide
I. Khái niệm về oxide
1. Khái niệm về oxide
– Oxide là hợp chất của hai nguyên tố, trong đó có một nguyên tố là oxygen.
2. Phân loại oxide
– Dựa vào thành phần nguyên tố, oxide có thể phân thành hai loại: oxide kim loại và oxide phi kim. Oxide kim loại được tạo thành từ phản ứng của kim loại với oxygen, ví dụ như phản ứng giữa Ba và O2 tạo ra BaO. Oxide phi kim được tạo thành từ phản ứng của phi kim với oxygen, ví dụ như phản ứng giữa C và O2 tạo ra CO2.
– Dựa vào tính chất hoá học, oxide có thể phân thành bốn loại: oxide acid, oxide base, oxide lưỡng tính và oxide trung tính.
– Quy tắc gọi tên oxide
+ Với nguyên tố chỉ có một hoá trị, ta đặt tên nguyên tố trước oxide, ví dụ như Sine oxide (ZnO).
+ Nguyên tố nhiều hoá trị: Tên nguyên tố (hoá trị của nguyên tố) + oxide
+ Cách đặt tên oxide của phi kim nhiều hoá trị:
+ (Tiền tố chỉ số nguyên tử của nguyên tố) Tên nguyên tố + (tiền tố chỉ số nguyên tử oxygen) oxide
+ (Tiền tố mono là một, đi là hai, trẻ là ba, tetra là bốn)
Ví dụ: FeO đọc là iron(II) oxide, CO đọc là carbon monoxide hoặc carbon(II) oxide, CO2 đọc là carbon dioxide hoặc carbon(IV) oxide
II. Tính chất hoá học
1. Oxide acid
– Oxide acid tác dụng với dung dịch base tạo thành muối và nước.
Ví dụ: CO2 + Ca(OH)2 → CaCO3 + H2O
– Khi sục từ từ khí CO2 vào dung dịch Ca(OH)2, ban đầu dung dịch vẩn đục do tạo muối CaCO3 không tan.
– Các oxide acid (như SO2, SO3, P2O5…) phản ứng với dung dịch base tạo thành muối và nước.
Ví dụ: SO2 + Ca(OH)2 → CaSO3 + H2O.
– Để kiểm tra tính chất của oxide acid, ta có thể thực hiện thí nghiệm bằng cách cho bột đá vôi và dung dịch hydrochloric acid vào ống nghiệm, sau đó dẫn khí carbon dioxide vào để tạo thành khí carbonic, quan sát hiện tượng xảy ra.
2. Oxide base
– Các oxide base (như CuO, Na2O, CaO…) phản ứng với dung dịch acid tạo thành muối và nước.
Ví dụ: CuO + H2SO4 → CuSO4 + H2O.
– Để kiểm tra tính chất của oxide base, ta có thể thực hiện thí nghiệm bằng cách cho bột CuO và dung dịch H2SO4 vào ống nghiệm, sau đó quan sát hiện tượng xảy ra.
Oxide lưỡng tính:
Oxide lưỡng tính (như Al2O3, ZnO…) tác dụng được với cả dung dịch acid và dung dịch base tạo thành muối và nước. Ví dụ: Al2O3 + 6HCl → 2AlCl3 + 3H2O.
3. Oxide trung tính
Oxide trung tính (như CO, N2O…) không tác dụng với dung dịch acid và dung dịch base, không tạo muối.
Sơ đồ tư duy KHTN 8 Bài 10: Oxide
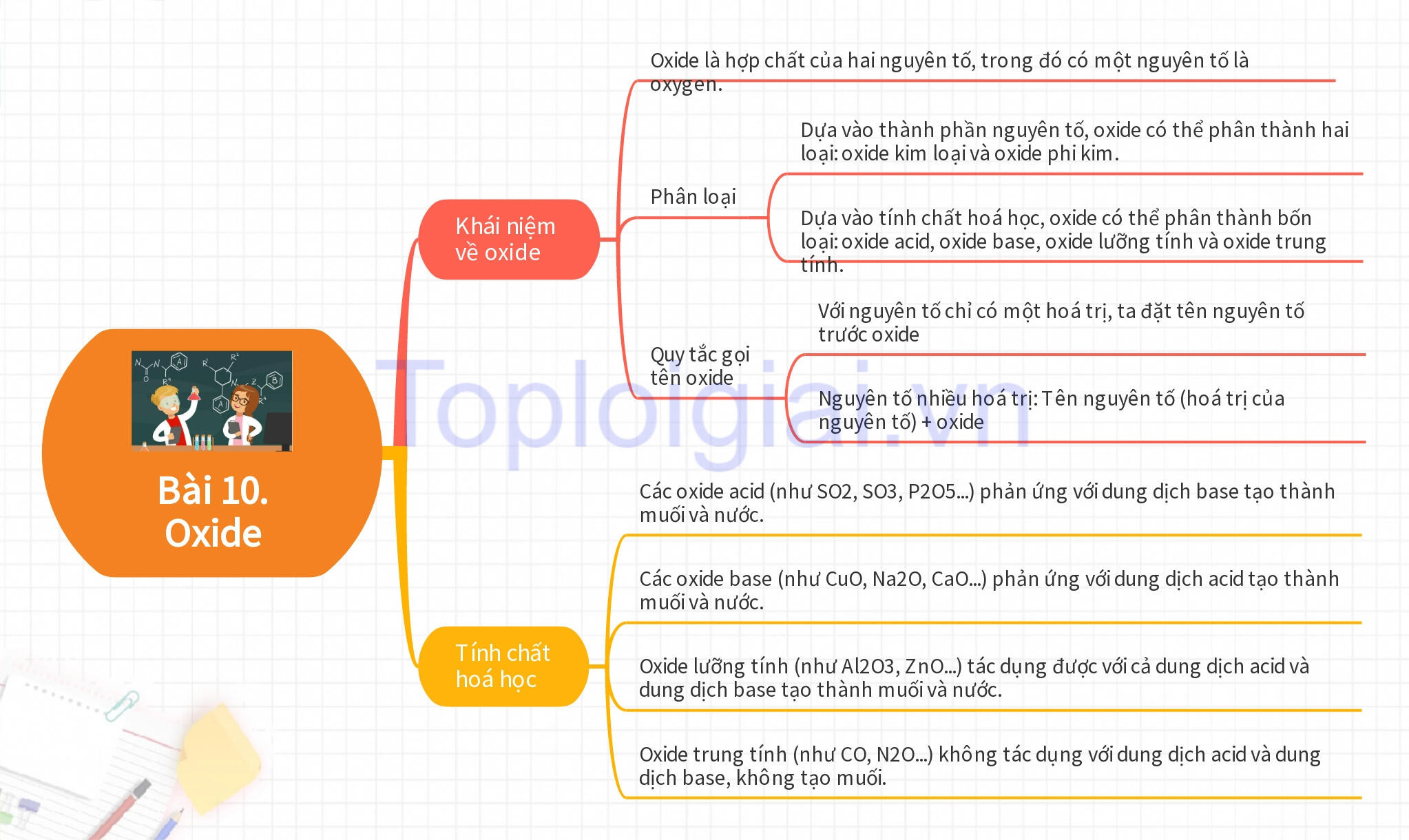
Xem thêm các bài giải SGK Khoa học tự nhiên lớp 8 Kết nối tri thức hay, chi tiết khác:
Bài 9: Base. Thang pH
Bài 10: Oxide
Bài 11: Muối
Bài 12: Phân bón hóa học
Bài 13: Khối lượng riêng