Lý thuyết Hóa học 12 Bài 22: Sơ lược về sự hình thành phức chất của ion kim loại chuyển tiếp trong dung dịch
A. Lý thuyết Sơ lược về sự hình thành phức chất của ion kim loại chuyển tiếp trong dung dịch
I. Sự hình thành phức chất aqua của cation kim loại chuyển tiếp trong dung dịch
– Khi tan trong nước, muối của các kim loại chuyển tiếp phân li thành các ion. Sau đó, cation kim loại chuyển tiếp (Mn+) thường nhận các cặp electron hóa trị riêng từ các phân tử H2O để hình thành các liên kết cho – nhận, tạo ra phức chất aqua theo phương trình hóa học tổng quát sau:;
Mn+(aq) + m H2O(l) [M(OH2)m]n+(aq)
+ Với: n là giá trị điện tích của cation kim loại M
m là số phối tử H2O
[M(OH2)m]n+ là công thức tổng quát của phức chất aqua của Mn+.
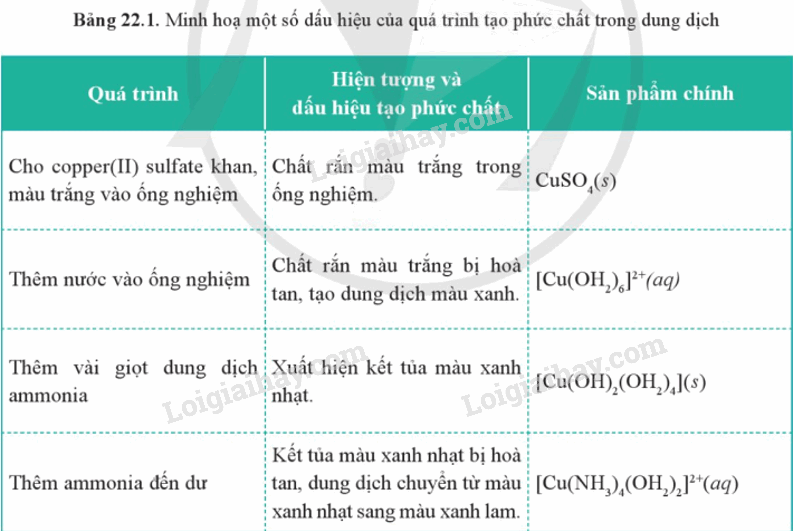
II. Dấu hiệu của phản ứng tạo phức chất trong dung dịch
Các phản ứng tạo phức chất thường có một số dấu hiệu dễ quan sát như sự biến đổi máu sắc, sự hòa tan, sự kết tủa. Trong các dấu hiệu trên, sự biến đổi màu sắc là phổ biến hơn cả
III. Phản ứng thay thế phối tử trong phức chất
Ở những điều kiện phù hợp, các anion và phân tử như OH–, X– (halide), NH3,…. Có thể thay thế được một, một số hoặc tất cả các phối tử trong phức chất
Ví dụ: [Cr(OH2)6]3+(aq) + 6OH–(aq) [Cr(OH)6]3-(aq) + 6H2O(l)
IV. Ứng dụng của phức chất
Các phức chất có nhiều ứng dụng trong hóa học, sản xuất và đời sống,…
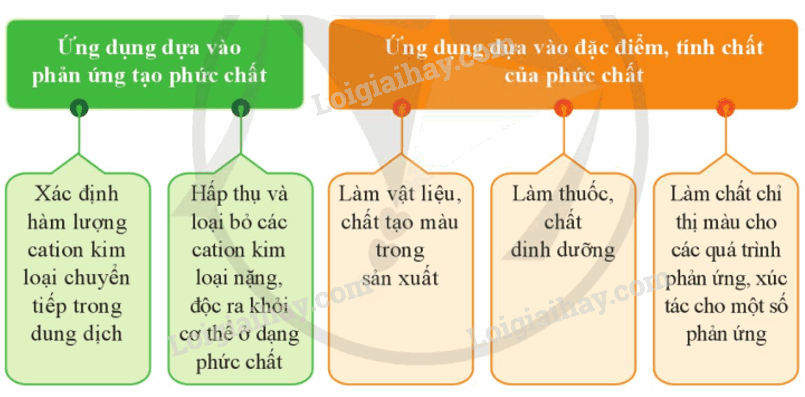
Sơ đồ tư duy Sơ lược về sự hình thành phức chất của ion kim loại chuyển tiếp trong dung dịch

B. Trắc nghiệm Sơ lược về sự hình thành phức chất của ion kim loại chuyển tiếp trong dung dịch
Phần I. Câu trắc nghiệm nhiều phương án lựa chọn. Mỗi câu hỏi chỉ chọn một phương án trả lời.
Câu 1: Các phối tử H2O trong phức chất [Ni(H2O)6]2+ có thể bị thế hết bởi sáu phối tử NH3 tạo thành phức chất là
A. [Ni(NH3)6]2+.
b. [Ni(NH3)2(H2O)4].
C. [Ni(NH3)(H2O)5]2+.
D. [Ni(NH3)5(H2O)]2+.
Hướng dẫn giải
Đáp án đúng là: A
Các phối tử H2O trong phức chất [Ni(H2O)6]2+ có thể bị thế hết bởi sáu phối tử NH3 tạo thành phức chất là [Ni(NH3)6]2+.
Câu 2: Phối tử H2O trong phức chất aqua [Cu(H2O)6]2+ có thể bị thế bởi 1 phối tử NH3 tạo thành phức chất là
A. [Cu(NH3)6]2+.
B. [Cu(NH3)2(H2O)5].
C. [Cu(NH3)(H2O)5]2+.
D. [Cu(NH3)(H2O)5]+.
Hướng dẫn giải
Đáp án đúng là: C
Phối tử H2O trong phức chất aqua [Cu(H2O)6]2+ có thể bị thế bởi 1 phối tử NH3 tạo thành phức chất là [Cu(NH3)(H2O)5]2+.
Câu 3: Phức chất [Cu(H2O)6]2+có màu xanh; phức chất [Cu(NH3)4(H2O)2] có màu xanh lam và phức chất [CuCl4]2- có màu vàng. Màu sắc của ba phức chất khác nhau là do chúng khác nhau về
A. nguyên tử trung tâm.
B. phối tử.
C. cả nguyên tử trung tâm và phối tử.
D. số lượng phối tử.
Hướng dẫn giải
Đáp án đúng là: B
Phức chất [Cu(H2O)6]2+có màu xanh; phức chất [Cu(NH3)4(H2O)2] có màu xanh lam và phức chất [CuCl4]2- có màu vàng. Màu sắc của ba phức chất khác nhau là do chúng khác nhau về phối tử.
Câu 4: Trong dung dịch, ion Fe3+ tồn tại dưới dạng phức chất aqua có sáu phối tử nước.
Cho các phát biểu sau:
a) Phức chất aqua có công thức hoá học là [Fe(H2O)6]3+.
b) Phức chất aqua có dạng hình học vuông phẳng.
c) 6 phối tử nước đã cho cặp electron chưa liên kết vào ion Fe3+.
d) Nguyên tử trung tâm trong phức chất aqua là Fe2+.
Số phát biểu đúng là:
A. 1.
B. 2.
C. 3.
D. 4.
Hướng dẫn giải
Đáp án đúng là: B
a) Đúng. Phức chất aqua có công thức hoá học là [Fe(H2O)6]3+.
b) Sai. Phức chất có dạng hình học là bát diện.
c) Đúng. 6 phối tử nước đã cho cặp electron chưa liên kết vào ion Fe3+.
d) Sai. Nguyên tử trung tâm trong phức chất aqua là Fe3+.
Vậy có 2 phát biểu đúng.
Câu 5: Trong phức chất [Co(H2O)6]2+, 2 phối tử H2O có thể bị thế bởi 2 phối tử OH. Phát biểu nào sau đây không đúng?
A. Phức chất tạo thành có 4 phối tử nước và 2 phối tử OH–.
B. Phức chất tạo thành có điện tích +2.
C. Phức chất tạo thành có nguyên tử trung tâm là Co2+.
D. Phức chất tạo thành là [Co(OH)2(H2O)4].
Hướng dẫn giải
Đáp án đúng là: B
Phức chất tạo thành là [Co(OH)2(H2O)4] không mang điện.
Câu 6: Dung dịch phức chất aqua không thể có màu xanh là
A. [Cr(H₂O)6]3+.
B. [Zn(H₂O)6]2+.
C. [Ni(H₂O)6]2+.
D. [Cu(H₂O)6]2+.
Hướng dẫn giải
Đáp án đúng là: B
Phức chất [Zn(H₂O)6]2+ không màu.
Câu 7: Phức chất nào sau đây của Cu2+ có màu vàng?
A. [Cu(H2O)6]2+.
B. [CuCl4]2-.
C. [Cu(NH3)4(H2O)2].
D. [Cu(OH)2(H2O)4].
Hướng dẫn giải
Đáp án đúng là: B
Phức chất [CuCl4]2- có màu vàng.
Câu 8: Nhỏ vài giọt dung dịch HCl đặc vào dung dịch CuSO4 tạo thành phức chất [CuCl4]2-. Dấu hiệu nào sau đây chứng tỏ phức chất [CuCl4]2- tạo thành?
A. Hoà tan kết tủa.
B. Đổi màu dung dịch từ màu xanh sang màu vàng.
C. Xuất hiện kết tủa.
D. Đổi màu dung dịch từ màu xanh lam sang màu vàng.
Hướng dẫn giải
Đáp án đúng là: B
Dấu hiệu chứng tỏ có phức chất [CuCl4]2- tạo thành: Đổi màu dung dịch từ màu xanh sang màu vàng.
Câu 9: Nhỏ vài giọt dung dịch NaOH loãng vào dung dịch CuSO4 tạo thành phức chất [Cu(OH)2(H2O)4]. Dấu hiệu nào sau đây chứng tỏ phức chất [Cu(OH)2(H2O)4] tạo thành?
A. Xuất hiện kết tủa màu xanh lam.
B. Hoà tan kết tủa.
C. Dung dịch chuyển từ màu xanh sang màu vàng.
D. Xuất hiện kết tủa màu xanh nhạt.
Hướng dẫn giải
Đáp án đúng là: D
Nhỏ vài giọt dung dịch NaOH loãng vào dung dịch CuSO4 tạo thành phức chất [Cu(OH)2(H2O)4], kết tủa màu xanh nhạt.
Câu 10: Phát biểu nào sau đây đúng?
A. Phức chất aqua là phức chất chứa phối tử NH3.
B. Phức chất của kim loại chuyển tiếp đều tan trong dung dịch.
C. Muối CuSO4 khan màu trắng khi tan vào nước tạo thành dung dịch có màu xanh do tạo thành phức chất aqua [Cu(H2O)612+.
D. Phức chất của kim loại chuyển tiếp đều có màu.
Hướng dẫn giải
Đáp án đúng là: C
Muối CuSO4 khan màu trắng khi tan vào nước tạo thành dung dịch có màu xanh do tạo thành phức chất aqua [Cu(H2O)612+.
Phát biểu A sai do phức chất aqua là phức chất chứa phối tử H2O.
Phát biểu B sai, ví dụ phức chất [Cu(OH)2(H2O)4], kết tủa màu xanh nhạt.
Phát biểu D sai, hầu hết các phức chất của kim loại chuyển tiếp có màu.
Phần II. Câu trắc nghiệm đúng sai. Trong mỗi ý a, b, c, d mỗi câu, hãy chọn đúng hoặc sai.
Câu 11: Cho các phát biểu sau về phức chất:
a. Trong dung dịch, các ion kim loại chuyển tiếp đều tạo phức chất aqua.
b. Các phối tử H2O trong phức chất aqua không thể bị thế bởi các phối tử khác.
c. Phức chất aqua của các ion kim loại chuyển tiếp hầu hết có dạng hình học bát diện.
d. Các phối tử trong phức chất có thể bị thay thế một phần hoặc thay thế hết bởi các phối tử khác.
Hướng dẫn giải
a. Đúng. Trong dung dịch, các ion kim loại chuyển tiếp đều tạo phức chất aqua.
b. Sai. Các phối tử H2O trong phức chất aqua có thể bị thế bởi các phối tử khác.
c. Đúng. Phức chất aqua của các ion kim loại chuyển tiếp hầu hết có dạng hình học bát diện.
d. Đúng. Các phối tử trong phức chất có thể bị thay thế một phần hoặc thay thế hết bởi các
Câu 12. Cho các phát biểu sau về phức chất:
a. Các phối tử trong phức chất chỉ có thể bị thế một phần bởi các phối tử khác.
b. Các phối tử trong phức chất chỉ có thể bị thế tất cả bởi các phối tử khác.
c. Tất cả các phức chất aqua đều kém tan trong nước.
d. Phức chất được dùng làm thuốc chữa bệnh ung thư với tên gọi thương phẩm là cisplatin có công thức hoá học là [PtCl2(NH3)2].
Hướng dẫn giải
a. Sai vì: Các phối tử trong phức chất có thể bị thay thế một phần hoặc bị thay thế tất cả thành các phối tử khác.
b. Sai vì: Các phối tử trong phức chất có thể bị thay thế một phần hoặc bị thay thế tất cả thành các phối tử khác.
c. Sai vì: Các phức chất aqua thường tan tốt trong nước.
d. Đúng.
Phần III. Câu trắc nghiệm yêu cầu trả lời ngắn
Câu 13: Phức chất [Pt(NH3)4]2+ có thể bị thế bởi 1 phối tử Cl–. Phức chất tạo thành có điện tích là bao nhiêu?
Hướng dẫn giải
Đáp án đúng là: +1.
Giải thích:
Phức chất [Pt(NH3)4]2+ có thể bị thế bởi 1 phối tử Cl–. Phức chất tạo thành có điện tích là +1.
Câu 14: Cisplatin là thế hệ đầu tiên trong số ba phức chất của Pt2+ được sử dụng trong điều trị ung thư. Nó được biết đến với vai trò to lớn trong điều trị ung thư buồng trứng, tinh hoàn, bàng quang, đầu, cổ,… Nhờ có cisplatin hơn 90
Giá trị của x là bao nhiêu?
Hướng dẫn giải
Đáp án đúng là: 1-
Giải thích:
Khi thay thế 1 phối tử Cl– trong phức chất [PtCl4]2- bằng phối tử NH3 ta được phức chất có điện tích là -1. Vậy x là 1-.
Câu 15: Cho cân bằng sau:
[CoCl4]²–(aq) + 6H₂O(1) [Co(H₂O)6]2+(aq) +4Cl–(aq)
(màu xanh chàm) (màu đỏ hồng)
Khi thêm dung dịch HCl, dung dịch sẽ có màu gì?
Hướng dẫn giải
Đáp án đúng là: màu xanh chàm
Giải thích:
Khi thêm HCl sẽ làm tăng nồng độ ion Cl–, nên cân bằng chuyển dịch sang chiều nghịch, màu dung dung dịch sẽ chuyển sàng xanh chàm.
Xem thêm các bài tóm tắt lý thuyết Hóa học lớp 12 Cánh diều hay, chi tiết khác:
Lý thuyết Bài 17: Nguyên tố nhóm IA
Lý thuyết Bài 18: Nguyên tố nhóm IIA
Lý thuyết Bài 19: Nước cứng và làm mềm nước cứng
Lý thuyết Bài 20: Sơ lược về kim lại chuyển tiếp dãy thứ nhất
Lý thuyết Bài 21: Sơ lược về phức chất
Lý thuyết Bài 22: Sơ lược về sự hình thành phức chất của ion kim loại chuyển tiếp trong dung dịch