Lý thuyết Hóa học 12 Bài 6: Amino acid
A. Lý thuyết Amino acid
I. Khái niệm, phân loại và danh pháp
1. Khái niệm
Khi thay thế một hay nhiều nguyên tử hydrogen trong phân tử ammonia bằng một hay nhiều gốc hydrocarbon thu được amine.
2. Phân loại
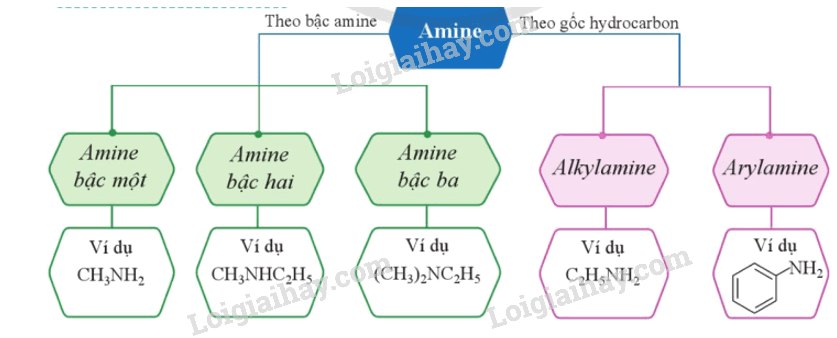
3. Danh pháp
Theo danh pháp gốc – chức, tên của amine được hình thành từ tên của các gốc hydrocarbon liên kết trực tiếp với nguyên tử nitrogen kèm theo tên chức amine
Theo danh pháp thay thế, các amine đơn chức được gọi tên như sau:
+ Amine bậc một: tên hydrocarbon (bỏ e) + vị trí nhóm –NH2 + amine
+ Amine bậc hai: N – tên gốc hydrocarbon + tên hydrocarbon mạch dài nhất (bỏ e) + vị trí nhóm chức amine + amine
+ Amine bậc ba: N – tên gốc hydrocarbon thứ nhất + N – tên gốc hydrocarbon thứ hai + tên hydrocarbon mạch dài nhất (bỏ e) + vị trí nhóm chức amine + amine.
II. Tính chất vật lý
– Methylamine, dimethylamine, trimethylamine và ethylamine là những chất khí ở điều kiện thường. Các amine có phân tử phối lớn hơn là chất lỏng hoặc chất rắn.
– Các amine có khối lượng phân tử thấp thường có mùi khó chịu
– Amine thường có nhiệt độ sôi cao hơn so với nhiệt độ sôi của các hydrocarbon có cùng số nguyên tử carbon hoặc có phân tử khối gần với chúng
III. Tính chất hóa học
1. Tính base và phản ứng tạo phức
– Dung dịch aniline trong nước không làm đổi màu quỳ tím, trong khi dung dịch các alkylamine có thể làm quỳ tím hóa xanh. Amine tác dụng với acid tạo thành muối. Các amine có khối lượng phân tử nhỏ có khả năng tác dụng với dung dịch muoói của một số kim loại tạo thành kết tủa hydroxide.
Ví dụ: C2H5NH2 + HCl [C2H5NH3]+Cl–
3C2H5NH2 + FeCl3 + 3H2OFe(OH)3 + 3[C2H5NH3]+Cl–
2. Tính khử
Alkylamine bậc một tác dụng với nitrous acid ở nhiệt độ thường tạo thành alcohol và giải phóng nitrogen
Ví dụ: C2H5NH2 + HONO C2H5OH + N2 + H2O
3. Phản ứng thế ở nhân thơm của aniline
Nhóm – NH2 trong phân tử aniline làm tăng mật độ electron trong vòng benzene, đặc biệt ở các vị trí ortho và para. Aniline dễ tham gia phản ứng với nước bromine tạo 2,4,6 – tribromoaniline kết tủa trắng.
IV. Ứng dụng và điều chế
1. Ứng dụng
– Hợp chất có nhóm chức amine được thấy trong thành phần của nhiều dược phẩm, thuốc bảo vệ thực vật,…
– Aniline là nguyên liệu quan trọng để tổng hợp phẩm nhuộm, chất hoạt động bề mặt.
2. Điều chế
a) Alkyl hóa ammonia
alkylamine được điều chế từ ammonia và dẫn xuất halogen.
Ví dụ: 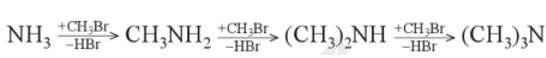
b) Khử hợp chất nitro
Arylamine thường được điều chế bằng cách khử dẫn xuất nitro tương ứng. Tác nhân khử thường dùng là kim loại trong hydrochloric acid
Ví dụ: ![]()
Sơ đồ tư duy Amino acid

B. Trắc nghiệm Amino acid
Phần I. Câu trắc nghiệm nhiều phương án lựa chọn.
Câu 1. Cho các chất sau: H2NCH2COOH (X), CH3COOH3NCH3 (Y), C2H5NH2 (Z), H2NCH2COOC2H5 (T). Dãy gồm các chất đều tác dụng được với dung dịch NaOH và dung dịch HCl là
A. X, Y, Z, T.
B. X, Y, T.
C. X, Y, Z.
D. Y, Z, T.
Hướng dẫn giải
Đáp án đúng là: B
Các chất X, Y, T tác dụng được với dung dịch NaOH và dung dịch HCl.
Phương trình hoá học:
– Chất X:
H2NCH2COOH + NaOH → H2NCH2COONa + H2O
H2NCH2COOH + HCl → ClH3NCH2COOH
– Chất Y:
CH3COOH3NCH3 + NaOH → CH3COONa + CH3NH2 + H2O
CH3COOH3NCH3 + HCl → CH3COOH + CH3NH3Cl
– Chất T:
H2NCH2COOC2H5 + NaOH → H2NCH2COONa + C2H5OH
H2NCH2COOC2H5 + HCl → ClH3NCH2COOC2H5
Câu 2. Amino acid X chứa một nhóm -NH2 và một nhóm -COOH trong phân tử. Y là ester của X với alcohol đơn chức, MY = 89. Công thức của X, Y lần lượt là
A. H2N-CH2-COOH, H2N-CH2-COOCH3.
B. H2N-[CH2]2-COOH, H2N-[CH2]2-COOC2H5.
C. H2N-[CH2]2-COOH, H2N-[CH2]2-COOCH3.
D. H2N-CH2-COOH, H2N-CH2-COOC2H5.
Hướng dẫn giải
Đáp án đúng là: A
MY = 89 ⇒ Y: C3H7O2N, Y là ester của amino acid ⇒ Y: H2N-CH2-COOCH3
⇒ X: H2N-CH2-COOH.
Câu 3. Kết quả thí nghiệm của các chất X, Y, Z với các thuốc thử được ghi ở bảng sau:
Chất | Thuốc thử | Hiện tượng |
X | Quỳ tím | Quỳ tím chuyển màu hồng |
Y | Dung dịch AgNO3 trong NH3 | Tạo kết tủa Ag |
Z | Nước bromine | Tạo kết tủa trắng |
Các chất X, Y, Z lần lượt là
A. ethyl formate, glutamic acid, aniline.
B. aniline, ethyl formate, glutamic acid.
C. glutamic acid, ethyl formate, aniline.
D. glutamic acid, aniline, ethyl formate.
Hướng dẫn giải
Đáp án đúng là: C
Z tạo kết tủa trắng với nước bromine ⇒ loại B, D
Y tráng bạc ⇒ loại A.
Vậy chọn C.
Câu 4. Chất nào sau đây vừa phản ứng được với dung dịch KOH, vừa phản ứng được với dung dịch HCl?
A. C2H5OH.
B. CH3COOH.
C. H2N-CH2-COOH.
D. C2H6.
Hướng dẫn giải
Đáp án đúng là: C
H2N-CH2-COOH + KOH → H2N-CH2-COOK + H2O
H2N-CH2-COOH + HCl → ClH3N-CH2-COOH
Câu 5. Phát biểu nào sau đây là sai khi nói về tính điện di của amino acid?
A. Trong dung dịch, dạng tồn tại chủ yếu của amino acid chỉ phụ thuộc vào pH của dung dịch.
B. Ở pH thấp, amino acid tồn tại chủ yếu ở dạng anion (tích điện âm), di chuyển về điện cực dương trong điện trường.
C. Ở pH cao, amino acid tồn tại chủ yếu ở dạng cation (tích điện dương), di chuyển về điện cực âm trong điện trường.
D. Tính điện di của amino acid là khả năng di chuyển khác nhau trong điện trường tùy thuộc vào pH của môi trường.
Hướng dẫn giải
Đáp án đúng là: A
Trong dung dịch, dạng tồn tại chủ yếu của amino acid phụ thuộc vào giá trị pH của môi trường và cấu tạo của mỗi amino acid.
Câu 6. Amino acid X có phân tử khối bằng 75. Tên của X là
A. alanine.
B. glycine.
C. valine.
D. lysine.
Hướng dẫn giải
Đáp án đúng là: B
Glycine (HOOC – CH2 – NH2) có phân tử khối bằng 75.
Câu 7. Chất X có công thức H2N-CH(CH3)COOH. Tên gọi của X là
A. glycine.
B. valine.
C. alanine.
D. lysine.
Hướng dẫn giải
Đáp án đúng là: C
Chất X có công thức H2N-CH(CH3)COOH có tên gọi là alanine.
Câu 8. Phần trăm khối lượng của nguyên tố nitrogen trong alanine là
A. 15,73