Câu hỏi:
Nung 0,935 gam quặng cromit với chất oxi hóa để oxi hóa toàn bộ crom thành CrO42-. Hòa tan sản phẩm vào nước, phân hủy hết chất oxi hóa, axit hóa dung dịch bằng H2SO4rồi thêm 50,0 ml dung dịch FeSO40,08M vào. Để chuẩn độ FeSO4dư cần 14,85 ml dung dịch KMnO40,004M. Hàm lượng crom có trong quặng là
A. 7,97%.
B.6,865%.
Đáp án chính xác
C.15,9%.
D.3,43%.
Trả lời:
Bước 1:Tính nFeSO4, nKMnO4
\({n_{F{{\rm{e}}^{2 + }}\left( {b{\rm{d}}} \right)}} = 0,05.0,08 = 0,004\left( {mol} \right)\)
\({n_{KMn{O_4}}} = 0,01485.0,004 = {5,94.10^{ – 5}}\left( {mol} \right)\)
Bước 2: Tính nCrO42-
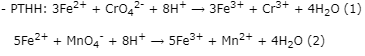
Theo (2) ⟹ nFe2+(dư)= 5.nMnO4-= 5.5,94.10-5= 2,97.10-4(mol)
⟹ nFe2+(pư)= 0,004 – 2,97.10-4= 3,703.10-3(mol)
Theo (1) ⟹ nCrO42-= 1/3.nFe2+(pư)= 1/3.3,703.10-3= 1,23433.10-3(mol)
⟹ mCr= 1,23433.10-3.52 = 0,064 gam.
Bước 3: Tính hàm lượng Crom trong quặng cromit
– %mCr=\(\frac{{0,064}}{{0,935}}.100{\rm{\% }}\; = {\rm{ }}6,845\% .\)
Đáp án cần chọn là: B
====== **** mời các bạn xem câu tiếp bên dưới **** =====
- Hoà tan 25 gam hỗn hợp X gồm FeSO4và Fe2(SO4)3vào nước, thu được 150 ml dung dịch Y. Thêm H2SO4(dư) vào 20 ml dung dịch Y rồi chuẩn độ toàn bộ dung dịch này bằng dung dịch KMnO40,1M thì dùng hết 30 ml dung dịch chuẩn. Phần trăm khối lượng FeSO4trong hỗn hợp X là – ĐGNL-HN
Câu hỏi:
Hoà tan 25 gam hỗn hợp X gồm FeSO4và Fe2(SO4)3vào nước, thu được 150 ml dung dịch Y. Thêm H2SO4(dư) vào 20 ml dung dịch Y rồi chuẩn độ toàn bộ dung dịch này bằng dung dịch KMnO40,1M thì dùng hết 30 ml dung dịch chuẩn. Phần trăm khối lượng FeSO4trong hỗn hợp X là
A. 68,4%.
Đáp án chính xác
B. 9,12%.
C.31,6%.
D.13,68%.
Trả lời:
Bước 1: Tính nFe2+ trong 20 ml dd Y
– nKMnO4= 0,1.0,03 = 0,003 mol
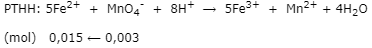
– Trong 20 ml dung dịch Y có 0,015 mol Fe2+
⟹ 150 ml dung dịch Y có x mol nFe2+
⟹ nFe2+ = 0,015.150/20 = 0,1125 mol
Bước 2: Tính %mFeSO4trong X
– mFeSO4= 0,1125.152 = 17,1 gam
→ %mFeSO4= (17,1/25).100% = 68,4%.
Đáp án cần chọn là: A====== **** mời các bạn xem câu tiếp bên dưới **** =====
- Để xác định nồng độ dung dịch NaOH người ta tiến hành như sau: Cân 1,26 gam axit oxalic ngậm nước (H2C2O4.2H2O) hòa tan hoàn toàn vào nước, định mức thành 100 ml. Lấy 10 ml dung dịch này thêm vào đó vài giọt phenolphthalein, đem chuẩn độ bằng dung dịch NaOH đến xuất hiện màu hồng (ở pH = 9) thì hết 17,5 ml dung dịch NaOH. Tính nồng độ dung dịch NaOH đã dùng. – ĐGNL-HN
Câu hỏi:
Để xác định nồng độ dung dịch NaOH người ta tiến hành như sau: Cân 1,26 gam axit oxalic ngậm nước (H2C2O4.2H2O) hòa tan hoàn toàn vào nước, định mức thành 100 ml. Lấy 10 ml dung dịch này thêm vào đó vài giọt phenolphthalein, đem chuẩn độ bằng dung dịch NaOH đến xuất hiện màu hồng (ở pH = 9) thì hết 17,5 ml dung dịch NaOH. Tính nồng độ dung dịch NaOH đã dùng.
A. 0,1143M.
Đáp án chính xác
B. 0,2600M.
C.0,1240M.
D.0,1600M.
Trả lời:
Bước 1: Tính n(COOH)2trong 10 ml dung dịch axit oxalic
– \({n_{{H_2}{C_2}{O_4}.2{H_2}O}} = \frac{{1,26}}{{90 + 18.2}} = 0,01\left( {mol} \right)\)
– 100 ml dung dịch axit oxalic chứa 0,01 mol (COOH)2
10 ml ⟶ 0,001 mol
Bước 2: Tính nNaOH
– Phenolphtalein xuất hiện màu hồng ở pH = 9 >7 ⟹ NaOH dư, (COOH)2hết
– Đặt nNaOH= x mol.
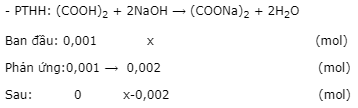
pH = 9 ⟹ pOH = 14 – 9 = 5 ⟹ [OH-]sau pư= 10-5
Bước 3: Tính CM NaOH
– Ta có:\({\left[ {O{H^ – }} \right]_{sau{\kern 1pt} pu}} = \frac{{x – 0,002}}{{(10 + 17,5){{.10}^{ – 3}}}} = {10^{ – 5}} \Rightarrow {\rm{ }}x{\rm{ }} = {\rm{ }}{2,000275.10^{ – 3}}.\)
\( \Rightarrow {\rm{ }}{C_{M{\rm{ }}NaOH}}\; = \frac{{{n_{NaOH}}}}{{{V_{dd{\kern 1pt} NaOH}}}} = \frac{{{{2,000275.10}^{ – 3}}}}{{{{17,5.10}^{ – 3}}}} = {\rm{ }}0,1143{\rm{ }}M.\)
Đáp án cần chọn là: A====== **** mời các bạn xem câu tiếp bên dưới **** =====
- Để xác định nồng độ dung dịch NaOH, người ta dùng dung dịch đó chuẩn độ 25,00 ml dung dịch H2C2O40,05M (dùng phenolphtalein làm chỉ thị). Khi chuẩn độ dùng hết 46,50 ml dung dịch NaOH. Nồng độ mol của dung dịch NaOH đó là – ĐGNL-HN
Câu hỏi:
Để xác định nồng độ dung dịch NaOH, người ta dùng dung dịch đó chuẩn độ 25,00 ml dung dịch H2C2O40,05M (dùng phenolphtalein làm chỉ thị). Khi chuẩn độ dùng hết 46,50 ml dung dịch NaOH. Nồng độ mol của dung dịch NaOH đó là
A. 0,027M.
B. 0,025M.
C.0,054M.
Đáp án chính xác
D.0,017M.
Trả lời:
Bước 1: Tính số mol NaOH
n(COOH)2= 0,025.0,05 = 0,00125 mol
Bước 2: Tính nồng độ NaOHPTHH: (COOH)2+ 2NaOH → (COONa)2+ 2H2O
nNaOH = 2n(COOH)2= 2.0,00125 = 0,0025 (mol)
⟹ CM NaOH= 0,025 : 0,0465 ≈ 0,054M
Đáp án cần chọn là: C====== **** mời các bạn xem câu tiếp bên dưới **** =====
- Để xác định nồng độ mol/l của dd K2Cr2O7người ta làm như sau:
Lấy 10 ml dung dịch K2Cr2O7cho tác dụng với lượng dư dung dịch KI trong môi trường axit sunfuric loãng dư. Lượng I2thoát ra trong phản ứng được chuẩn độ bằng lượng vừa đủ là 18 ml dung dịch Na2S2O30,05M.
Biết các phản ứng hóa học xảy ra:
(1) 6KI + K2Cr2O7+ 7H2SO4→ 4K2SO4+ Cr2(SO4)3+ 3I2+ 7H2O;
(2) I2+ 2Na2S2O3→ 2NaI + Na2S4O6.
Nồng độ mol/l của K2Cr2O7là – ĐGNL-HN
Câu hỏi:
Để xác định nồng độ mol/l của dd K2Cr2O7người ta làm như sau:
Lấy 10 ml dung dịch K2Cr2O7cho tác dụng với lượng dư dung dịch KI trong môi trường axit sunfuric loãng dư. Lượng I2thoát ra trong phản ứng được chuẩn độ bằng lượng vừa đủ là 18 ml dung dịch Na2S2O30,05M.
Biết các phản ứng hóa học xảy ra:
(1) 6KI + K2Cr2O7+ 7H2SO4→ 4K2SO4+ Cr2(SO4)3+ 3I2+ 7H2O;
(2) I2+ 2Na2S2O3→ 2NaI + Na2S4O6.
Nồng độ mol/l của K2Cr2O7làA. 0,02M.
B. 0,03M.
C.0,015M.
Đáp án chính xác
D.0,01M.
Trả lời:
Bước 1: Tính số mol của Na2S2O3
nNa2S2O3= 0,018.0,05 = 9.10-4mol
Bước 2: Viết phương trình phản ứng, tính số mol các chất theo PTHH
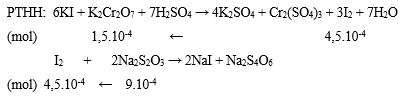
Bước 3: Tính CMcủa K2Cr2O7
⟹ CM K2Cr2O7= 1,5.10-4/0,01 = 0,0015M.
Đáp án cần chọn là: C====== **** mời các bạn xem câu tiếp bên dưới **** =====
- Để xác định nồng độ dung dịch H2O2, người ta hòa tan 0,5 gam nước oxi già vào nước, thêm H2SO4tạo môi trường axit. Chuẩn độ dung dịch thu được cần vừa đủ 10 ml dung dịch KMnO40,1M. Xác định hàm lượng H2O2trong nước oxi già.
Biết phản ứng chuẩn độ: 5H2O2+ 2KMnO4+ 3H2SO4⟶ K2SO4+ 2MnSO4+ 5O2+ 8H2O. – ĐGNL-HN
Câu hỏi:
Để xác định nồng độ dung dịch H2O2, người ta hòa tan 0,5 gam nước oxi già vào nước, thêm H2SO4tạo môi trường axit. Chuẩn độ dung dịch thu được cần vừa đủ 10 ml dung dịch KMnO40,1M. Xác định hàm lượng H2O2trong nước oxi già.
Biết phản ứng chuẩn độ: 5H2O2+ 2KMnO4+ 3H2SO4⟶ K2SO4+ 2MnSO4+ 5O2+ 8H2O.A.9%.
B.17%.
Đáp án chính xác
C.12%.
D.21%.
Trả lời:
Bước 1: Tính số mol của H2O2
nKMnO4=0,01.0,1=0,001(mol)nKMnO4=0,01.0,1=0,001(mol)
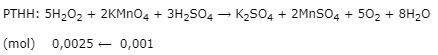
Bước 2: Xác định hàm lượng H2O2
\({m_{{H_2}{O_2}}} = 0,0025.34 = 0,085\left( g \right)\)
⟹ Hàm lượng H2O2trong nước oxi già là\(\frac{{0,085}}{{0,5}}.100{\rm{\% }} = 17{\rm{\% }}\)
Đáp án cần chọn là: B====== **** mời các bạn xem câu tiếp bên dưới **** =====
