1. Giải bài 1 trang 155 SGK Hóa học 12
Viết phương trình hóa học của các phản ứng trong quá trình chuyển hóa sau:
Cr Cr2O3
Cr2(SO4)3
Cr(OH)3
Cr2O3
Phương pháp giải
Để viết phương trình hóa học của các phản ứng trong quá trình chuyển hóa trên cần nắm rõ tính chất hóa học của crom và hợp chât của crom.
Hướng dẫn giải
Phương trình hóa học của các phản ứng:
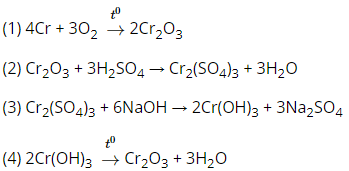
2. Giải bài 2 trang 155 SGK Hóa học 12
Cấu hình electron của Cr3+ là
A. [Ar]3d5.
B. [Ar]3d4.
C. [Ar]3d3.
D. [Ar].
Phương pháp giải
Để chọn đáp án đúng ta viết cấu hình electron của Cr
Trừ đi 3 electron lớp ngoài cùng của Cr => cấu hình của Cr3+
Hướng dẫn giải
Cấu hình e của Cr ( Z = 24): [Ar] 3d54s1
→ Cấu hình electron của Cr3+ là [Ar]3d3
Vậy đáp án đúng là C.
3. Giải bài 3 trang 155 SGK Hóa học 12
Số oxi hóa đặc trưng của crom là
A. +2, +4, +6.
B. +2, +3, +6.
C. +1, +2, +4, +6.
D. +3, +4, +6.
Phương pháp giải
Để xác định số oxi hóa của crom ta cần nắm rõ lý thuyết về crom.
Hướng dẫn giải
Số oxi hóa đặc trưng của crom là +2, +3, +6
Đáp án đúng là B.
4. Giải bài 4 trang 155 SGK Hóa học 12
Hãy viết công thức của một số muối crom trong đó nguyên tố crom
a) Đóng vai trò cation.
b) Có trong thành phần của anion.
Phương pháp giải
Để trả lời câu hỏi trên cần nắm được lý thuyết về hợp chất của crom.
Hướng dẫn giải
Câu a
Crom đóng vai trò cation: CrCl2, Cr2(SO4)3
Câu b
Crom có trong thành phần của anion: Na2CrO4, K2Cr2O7
5. Giải bài 5 trang 155 SGK Hóa học 12
Khi nung nóng 2 mol natri đicromat người ta thu được 48 gam oxi và 1 mol crom(III) oxit. Hãy viết phương trình hóa học của phản ứng và xét xem natri đicromat đã bị nhiệt phân hoàn toàn hay chưa?
Phương pháp giải
Dựa vào phương trình:Na2Cr2O7 → Na2O + Cr2O3 + 3/2O2
Tính toán theo số mol của Cr2O3 và O2
Hướng dẫn giải
Ta có:
\({n_{{O_2}}} = \frac{{48}}{{32}} = 1,5\) (mol)
⇒ Phương trình hóa học:
Na2Cr2O7 → Na2O + Cr2O3 + 3/2O2
1 1 1 1,5(mol)
nNa2Cr2O7 dư = 2 – 1 = 1 mol
→ Na2Cr2O7 chưa bị phân hủy hết
Vậy Na2Cr2O7 chưa bị nhiệt phân hoàn toàn.
